marqueurs sanguins tumoraux en cancérologie digestive gastro casa procto casa-الدلائل الدموية المشخصة لأورام سرطان القناة الهضمية:
Les marqueurs sanguins tumoraux en cancérologie digestive-الدلائل الدموية المشخصة لأورام سرطان القناة الهضمية
الملخص:
يعتقد مثل أغلبية الدلائل البيولوجية في مجال السرطان و خارجه ، الدليل الأسمى أهمية،دليل كفيل بتوفير الكشف الصحيح un diagnostic de certitude . و هو كذلك الدليل الذي تمكن إعادته و يخبر عن مستقبل تطور الداء . و يعتقد بالتالي الدليل المختار.
و بعبارة ثالثة تعرف كيفية qualité الدليل البيولوجي لخصوصيته و حساسيته و قدرته على الإخبار حول التطور في المستقبل caractère pronostique و ليس من شك في فائدة الأوصاف الإضافية التي يتسم بها الدليل الجيد مثل سهولة التوفر على الفحص ، و تجرده من الهجومية critère non invasif ، و كذلك الثمن ، كلها دلائل مهمة غير أننا لن نستدرجها في موضوعنا .
تشمل الدلائل الدموية الرئيسية لتشخيص سرطان القناة الهضمية المستضاد السرطاني الجيني أو أ س أACE) )antigène carcino-embryonnaireأو مستضاد الكارسينوامبريوتير و دليل آلفا فيتوب روتين alphafoetoprotéine ( AFP) و دليل س أ19.9 ca 19.9/ إنها مواد أبروتينيةsubstances protéiques
داخلية ، بتكاثر إفرازها أثناء الإصابة و خاصة خلال تنشيط بعض الجينات activationde gène في المجال السرطاني ، و إن فائدة استعمال تلك الدلائل الثلاثة اللواتي يتم اللجوء إليها بطرقة روتينية سريريه ظلت موضوع نقاش بالنسبة للفائدة و ربماالمنفعة و أن فائدتها أخذت في التطور مع مرور الأيام لان تأثيرها جد مرتبط بتطور أخذ المواقف السريرية و العلاجية و التقنية.و يشير تعقد التقييم إلى اختلاف الحالات الأكثر ترددا و استدراج المفاهيم من أد غنى littérature riche .
الملاحظة السريرية الأولى:
لنأخذ مثل شخص بالغ من العمر 70 سنة سبق له أن تعرض لجراحة سرطان القولون السيني cancer du colon sigmoïde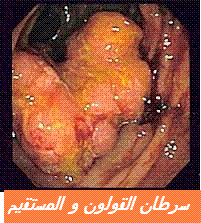 خلال 8 أشهر السالفة. سرطان من صنف الادينوكارسينوم adénocarcinome المرتب pTN1 ( درجة TNMIII) و حضي المصاب ب 12 حصة من الكيميوتيرابي الإضافية بعقار FOLFOX4 ( مدة 6 أشهر من العلاج ) . و يوجد المصاب حاليا في حالة جيدة ممتازة و ظل فحصه السريري عاديا و أصبح فحص عامل ACE عاديا بعدما كان مرتفعا قبل العملية الجراحية يجب أن يتم المراقبة السريرية كل 3 أشهر حيث تشمل الفحص بالايكوجرافي كل 3 أشهر و فحص الصدر بأشعة الراديوم كل 6 أشهر . و مادام امتداد أعمار هؤلاء المصابين لا يفوق 5 سنوات لنسبة تربو عن 65% و يتعرضون لتنقل الداء
خلال 8 أشهر السالفة. سرطان من صنف الادينوكارسينوم adénocarcinome المرتب pTN1 ( درجة TNMIII) و حضي المصاب ب 12 حصة من الكيميوتيرابي الإضافية بعقار FOLFOX4 ( مدة 6 أشهر من العلاج ) . و يوجد المصاب حاليا في حالة جيدة ممتازة و ظل فحصه السريري عاديا و أصبح فحص عامل ACE عاديا بعدما كان مرتفعا قبل العملية الجراحية يجب أن يتم المراقبة السريرية كل 3 أشهر حيث تشمل الفحص بالايكوجرافي كل 3 أشهر و فحص الصدر بأشعة الراديوم كل 6 أشهر . و مادام امتداد أعمار هؤلاء المصابين لا يفوق 5 سنوات لنسبة تربو عن 65% و يتعرضون لتنقل الداء 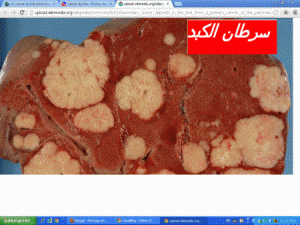 métastases إلى الكبد بنسبة 80% مصحوبا أو غير مصحوب بإصابة الرئة ، فان المراقبة تتركز غالبا على الكبد من تلك المراقبة على كشف الانتكاس المبكر الكفيل باللجوء إلى الاستئصال الجراحي الشامل الذي يحقق الشفاء و امتداد الأعمار إلى 5 سنوات بنسبة تربو عن 30% ، و قد يتعرض للانتكاس التنقليrécidive métastatique بنسبة تربو عن 25% و الانتكاس ألموقعي récidive locale بنسبة 58% .
métastases إلى الكبد بنسبة 80% مصحوبا أو غير مصحوب بإصابة الرئة ، فان المراقبة تتركز غالبا على الكبد من تلك المراقبة على كشف الانتكاس المبكر الكفيل باللجوء إلى الاستئصال الجراحي الشامل الذي يحقق الشفاء و امتداد الأعمار إلى 5 سنوات بنسبة تربو عن 30% ، و قد يتعرض للانتكاس التنقليrécidive métastatique بنسبة تربو عن 25% و الانتكاس ألموقعي récidive locale بنسبة 58% .
خلاصة القول: تهدف مراقبة فحص أ س أ ACE في إطار سرطان القولون المستأصل cancer colorectal réséqué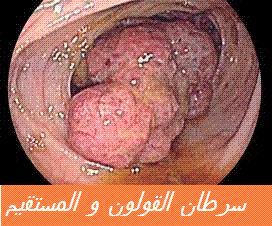 غالبا إلى كشف الانتكاس المبكر الذي يحتمل أن يؤدي الى الاستئصال الشامل . يعد رجوع عامل أ س أ إلى مقداره العادي بعد الجراحة ، نبئا مهما غير انه لا يتدخل في أخد قرار العلاج و لا في إستراتيجية المراقبة . يعتقد ارتفاع أ س أ ACE أول دليل يشير إلى الإصابة بالانتكاس بنسبة تتراوح ما بين 60 و 70% من الحالات و نسبة الأعراض الراديولوجية و / أو السريرية ب 3 أو 8 أشهر . غير أن بعض الدراسات الطبية لم تؤكد الدور الذي تلعبه مراقبة لعامل أ ج ج IgG .
غالبا إلى كشف الانتكاس المبكر الذي يحتمل أن يؤدي الى الاستئصال الشامل . يعد رجوع عامل أ س أ إلى مقداره العادي بعد الجراحة ، نبئا مهما غير انه لا يتدخل في أخد قرار العلاج و لا في إستراتيجية المراقبة . يعتقد ارتفاع أ س أ ACE أول دليل يشير إلى الإصابة بالانتكاس بنسبة تتراوح ما بين 60 و 70% من الحالات و نسبة الأعراض الراديولوجية و / أو السريرية ب 3 أو 8 أشهر . غير أن بعض الدراسات الطبية لم تؤكد الدور الذي تلعبه مراقبة لعامل أ ج ج IgG .
فليس من فرق بين المراقبة الكثيفة و الخفيفة في مقارنة امتداد أعمار المصابين الى 5 سنوات . يحتمل ان تدخل نسبة الاستئصال الثانوي résection secondaire للاورام المتنقلة ، تدخل تحسينات . و تمثل فائدة مهمة لا يمكن إهمالها .
و خلاصة القول : تكمن فائدة فحص أ س أ في التشخيص المبكر بعد استئصال سرطان القولون ، في التشخيص المبكر للانتكاسات .يحتمل استئصالها في الوقت الذي تظل فيه الفحوص التصويرية التقليدية عادية . إن ظهور فحص التوموجرافي بواسطة إشعاع البوسترون tomoghraphie par émission des positrons( TEP-scan) كفيل بتشخيص ارتفاع ميتابوليزم الورميhyper métabolisme tumoral . لقد أصبح اللجوء الى هذا الفحص أمرا منتظما أو بعد ملاحظة ارتفاع أ س أ.
الملاحظة السريرية الثانية:
تهم هاته الملاحظة رجلا في سن 74 مدمنا على استهلاك الكحول و التدخين بصفة مزمنة ، مصاب بتشمع كبدي تضاعف بتنقل سرطاني cirrhose secondaire
و التدخين بصفة مزمنة ، مصاب بتشمع كبدي تضاعف بتنقل سرطاني cirrhose secondaire و فشل كبدي أدى إلى تدهور صحة المصاب . و لا تشمل الأعراض السريرة سوى الانتفاخ الكبدي المنفرد hépatomégalie isolée و تشمل مجموعة الفحوص التي تم اللجوء إليها :
و فشل كبدي أدى إلى تدهور صحة المصاب . و لا تشمل الأعراض السريرة سوى الانتفاخ الكبدي المنفرد hépatomégalie isolée و تشمل مجموعة الفحوص التي تم اللجوء إليها :
الفحوص البيولوجية و التصويرية و الايكوجرافي أو اسكانير البطن و الحوض و الصدر scanner thoraco-abdomino-pélvien . و يتم فحص الكبد بالرنين المغناطيسي IRM hépatique حيث يشخص وجود نسيج كبدي غير متجانس و كبد غير متساوي الحروف à bords irréguliers مصاب بأورام nodules. يحتمل أن يرتفع فحص أ س أ خاصة أثناء الإصابة بسرطان الثدي cancer du sein المعدة و القولون و المستقيم.
و يشير فحص س أ 19.9 CA 19.9/ إلى أن الإصابة بسرطان الجهاز الصفراوي و البنكرياس sphère biliopancréatique . أما فحص الفا فيتوبروتيين AFP فيسير للإصابة بالسرطان الكبدي الأصلي cancer primitif du foie أو الأورام الجيرمانية tumeurs girminalls . لقد تم وصف مستضاد ACE سنة 1965 من صنف كولد و افيردمان Gold and freedman و تفرز بعض أصناف الأدينوكارسينوم من أصول هضمية . و تعتقد فائدة الاحتمال متعددة :
sphère biliopancréatique . أما فحص الفا فيتوبروتيين AFP فيسير للإصابة بالسرطان الكبدي الأصلي cancer primitif du foie أو الأورام الجيرمانية tumeurs girminalls . لقد تم وصف مستضاد ACE سنة 1965 من صنف كولد و افيردمان Gold and freedman و تفرز بعض أصناف الأدينوكارسينوم من أصول هضمية . و تعتقد فائدة الاحتمال متعددة :
-الدور تجاه المستقبل Rôle pronostique
يستمر وجود الارتفاع ما بين 4 و 6 أسابيع بعد استئصال السرطان القولوني أو الاستئصال الشامل للوحدات السرطانية المتنقلة و يرتبط ذلك عامة باستدامة وجود نسيج سرطاني ووجود وحدات متنقلة لم يتم تشخيصها بالتصوير infra radiologique و تنبئ بخبر سيء pronostic péjoratif. يجب التفكير في دور الارتفاع قبل عملية استئصال سرطان القولون و المستقيم و خاصة في حالة عدم الإصابة العقيدية en cas de non envahissement ganglionnaire يمثل إذا فحص أ س أ دليلا يشير لتطور سرطان القولون و المستقيم دون أن يساهم في اختيار إستراتيجية العلاج . و لهذا فليس من الضرورة بما كان تقييمه بطريقة منتظمة .
– دور الإخبار حول فعالية العلاج .
– يساعد ارتفاع ACE أثناء فحصين متتابعين عند الشخص الخاضع للعلاج بالكيميوتيرابي ، يساعد على مراقبة تطور الداء . و يشير بالتالي لعدم فعالية العلاج échappement thérapeutique . و يعتقد افحص جد مفيد في حالة الإصابة بالسرطان العسير التشخيص مثل سرطان الأحشاء الباطنية carcinosepéritonéale. أما انخفاض ACE فيعتقد بالعكس أثناء العلاج السرطاني دليلا متفائلا يحسن فعالية العلاج.
– و خلاصة القول: يجب أن لا يتم اللجوء لفحص ACE سوى في حالة الشك في كفاءة الفحوص التصويرية en cas de doute de l’imagerie أو في حالة الداء صعب التشخيص maladie non mesurable
– دور التشخيص rôle diagnostique .
يتيح المجال الورمي le spectre tumoral لكل دليل توجه الكشف ، و لكن نادرا ما يستطيع تأكيده . فحص ACEيهم خاصة الورم من أصل هضمي قولوني أو ورم المعدة أو الثدي carcinome mammair e الورم الجد مميز الذي لازال محتفظا على قدرة الإفراز . تعتقد حساسية فحص ACE في تقييم و احتمال الإصابة بالأورام المتنقلة من سرطان القولون و المستقيم ، يعتقد ما بين 50 و 90% و ترتفع قيمة فحص ACE كلما أضيف إليها التصوير الكبدي و فحص جما ج ت gamma-GT و بالرغم من ذلك يظل الفحص النسيجي الحجر الأساسي للكشف . أما وجود ورم كبدي منفرد زيادة عن الارتفاع المتوسطي لفحص ACE فيلاحظ في حالة التدخين tabagisme و فشل الكلى المزمنinsuffisancerénale chronique أو كذلك الأمراض الالتهابية المزمنة ( الايجابيات المغلوطة les faux positifs ) . و كذلك فان فحص س أ 19.9 CA 19.9/ دليل يشير لوجود أورام هضمية tumeurs digestives من أصول صفراوية خاصة أو بنكرياسية origine bilio-pancréatique. يحتمل أن يغدو مسئولا على الارتفاع المتوسط لفحص CA19.9 وجود الركود الصفراوي cholestase و اليرقان
e الورم الجد مميز الذي لازال محتفظا على قدرة الإفراز . تعتقد حساسية فحص ACE في تقييم و احتمال الإصابة بالأورام المتنقلة من سرطان القولون و المستقيم ، يعتقد ما بين 50 و 90% و ترتفع قيمة فحص ACE كلما أضيف إليها التصوير الكبدي و فحص جما ج ت gamma-GT و بالرغم من ذلك يظل الفحص النسيجي الحجر الأساسي للكشف . أما وجود ورم كبدي منفرد زيادة عن الارتفاع المتوسطي لفحص ACE فيلاحظ في حالة التدخين tabagisme و فشل الكلى المزمنinsuffisancerénale chronique أو كذلك الأمراض الالتهابية المزمنة ( الايجابيات المغلوطة les faux positifs ) . و كذلك فان فحص س أ 19.9 CA 19.9/ دليل يشير لوجود أورام هضمية tumeurs digestives من أصول صفراوية خاصة أو بنكرياسية origine bilio-pancréatique. يحتمل أن يغدو مسئولا على الارتفاع المتوسط لفحص CA19.9 وجود الركود الصفراوي cholestase و اليرقان  ictère و داء الهيموكروماتوز hémochromatose أو إصابة البنكرياس بورم حميد. و إن هذا الارتفاع المتوسط ( يفوق الأرقام العادية بأقل من 3 مرات ) ينقص من خصوصية الفحص بالنسبة للمقادير العالية و ترتفع حساسية الفحص إلى 80% بالنسبة لأورام الكولانجيوكارسينوم cholangiocarcinome و كرسينوم المرارة carcinome vésiculaire . و يعتقد الفحص قليل الحساسية بالنسبة لسرطان القولون و المستقيم سرطان المعدة cancer gastrique وسرطان الخلايا الكبدية carcinome hépatocellulaire . و يتركز هنا كذلك على تأكيد صحة الكشف النسيجي le diagnostic histologique . و إن إضافة التشمع الكبدي أو وجود التهاب كبدي مزمن يعتقد دليلا أساسيا يتيح التفكير في احتمال وجود سرطان الخلايا الكبدية . يعتقد ارتفاع فحص ألفا فيتوبروتيين AFP مرتبطا بنسبة حجم الورم و ليست حساسية الكشف مرتفعة بالنسبة للأورام الصغيرة الحجم أقل من 2 سنتم .
ictère و داء الهيموكروماتوز hémochromatose أو إصابة البنكرياس بورم حميد. و إن هذا الارتفاع المتوسط ( يفوق الأرقام العادية بأقل من 3 مرات ) ينقص من خصوصية الفحص بالنسبة للمقادير العالية و ترتفع حساسية الفحص إلى 80% بالنسبة لأورام الكولانجيوكارسينوم cholangiocarcinome و كرسينوم المرارة carcinome vésiculaire . و يعتقد الفحص قليل الحساسية بالنسبة لسرطان القولون و المستقيم سرطان المعدة cancer gastrique وسرطان الخلايا الكبدية carcinome hépatocellulaire . و يتركز هنا كذلك على تأكيد صحة الكشف النسيجي le diagnostic histologique . و إن إضافة التشمع الكبدي أو وجود التهاب كبدي مزمن يعتقد دليلا أساسيا يتيح التفكير في احتمال وجود سرطان الخلايا الكبدية . يعتقد ارتفاع فحص ألفا فيتوبروتيين AFP مرتبطا بنسبة حجم الورم و ليست حساسية الكشف مرتفعة بالنسبة للأورام الصغيرة الحجم أقل من 2 سنتم .
ترتفع الحساسية إلى 100% حينما تفوق مقاديرها 400 وحدة و يكون الورم غنيا بالأوعية الدموية tumeur hyper vascularisée حسب التشخيص بجهاز اسكانير المصحوب بتلقيح مادة الكونتراست scanner avec injection و الفحص بالرنين المغناطيسي IRM. و بالرغم من أن فحص الخزعة ظل يحتفظ به في حالة الشك فان ضرورة اللجوء و العودة إليه أصبحت امرأ قائما إزاء العلاج الموجه thérapeutique cible . الذي يتطلب مفهوما دقيقا لبيولوجية الورم . و لا يمكن الاعتماد من جهة ثانية على فحص AFP في تشخيص الأورام الكبدية الدقيقة المبتكرة التطور . و في الواقع فان كشف الأورام الكبدية ذات حجم يقل عن 20 سنتم متطورة في كيد متشمع تشير في أكثر من نصف الحالات إلى الإصابات الحميدة ( الأورام الريجينرية nodules de régénération و الأورام الديسبلازية nodules dysplasiques و في بعض الحالات الأورام الصفراوية الخبيثة tumeurs biliaires malignes ) و لا يتم اللجوء للفحص الهجومي النسيجي سوى في حالة ورم ذي حجم يفوق 1 سنتم .
الخاتمة :
تقترح الأبحاث العلمية الاستعمال المفرط للعوامل الورمية الذي يمثل بالإضافة للتاثير الطبي و الاقتصادي منبعا للتغليط و في بعض الحالات مبعثا لزرع الفزع في الطبيب و المصاب معا . و لا تتيح خصوصية الفحوص استبدال الكشف النسيجي .
و لا يجوز الاستعمال الروتيني لعوامل AFP وACE وCA19.9 في هذا الإطار و يجب أن لا يتم الاحتفاظ بتلك العوامل لتشخيص الأورام دون قصد لتقييم فعاليةالعلاج.
http://www.docteuramine.com/
Gastro casa procto